近期,國產(chǎn)胰島素龍頭通化東寶再傳捷報,URAT1抑制劑(THDBH130片)Ⅱ期臨床試驗完成首例受試者入組。近年來,通化東寶持續(xù)加碼研發(fā),猛攻創(chuàng)新藥,實現(xiàn)對胰島素類似物注射液、GLP-1受體激動劑、高臨床價值口服降糖藥品研發(fā)的全覆蓋。2022年拿下3款重磅新品;2款產(chǎn)品報產(chǎn)在審,20億大品種利拉魯肽注射液搶國產(chǎn)首家。此外,公司多渠道布局,國產(chǎn)胰島素揚帆出海,GLP-1/GIP雙受體激動劑(注射用THDBH121)申報臨床、人胰島素注射液在歐盟申報上市均獲受理。
猛攻創(chuàng)新藥,胰島素、GLP-1、口服降糖藥全覆蓋

來源:米內(nèi)網(wǎng)新版數(shù)據(jù)庫
近日,通化東寶發(fā)布公告,其全資子公司東寶紫星(杭州)生物醫(yī)藥的化藥1類新藥URAT1抑制劑(THDBH130片)已經(jīng)順利完成I期臨床試驗,已啟動中國II期臨床試驗,并于近日成功完成首例受試者入組。THDBH130片是一種特異性作用于尿酸排泄通路的高活性、高選擇性、高安全性的尿酸轉(zhuǎn)運體URAT1抑制劑,I期臨床試驗結(jié)果顯示其具有低系統(tǒng)暴露、高藥理學(xué)活性、餐后給藥更優(yōu)的降尿酸效應(yīng)特點,具有良好的安全性及耐受性。
目前,以URAT1為靶點的排尿酸藥物主要有苯溴馬隆和雷西那德。米內(nèi)網(wǎng)數(shù)據(jù)顯示,2021年三大終端6大市場(統(tǒng)計范圍見文末)抗痛風(fēng)制劑合計銷售規(guī)模超過20億元,苯溴馬隆是TOP2品種,雷西那德未在國內(nèi)上市。
據(jù)了解,此次啟動“一項在成人高尿酸血癥伴或不伴痛風(fēng)患者中評價THDBH130片的安全性、耐受性,初步臨床有效性及藥代/藥效動力學(xué)特征的多中心、隨機、雙盲、安慰劑和苯溴馬隆對照IIa期臨床研究”,主要目的是評估口服THDBH130片安全性、耐受性和初步有效性;次要目的包括評估降尿酸作用、對患者痛風(fēng)發(fā)作的影響及藥代/藥效動力學(xué)特征。截至公告日,公司在該項目中研發(fā)投入約4023.52萬元。
通化東寶部分在研項目情況
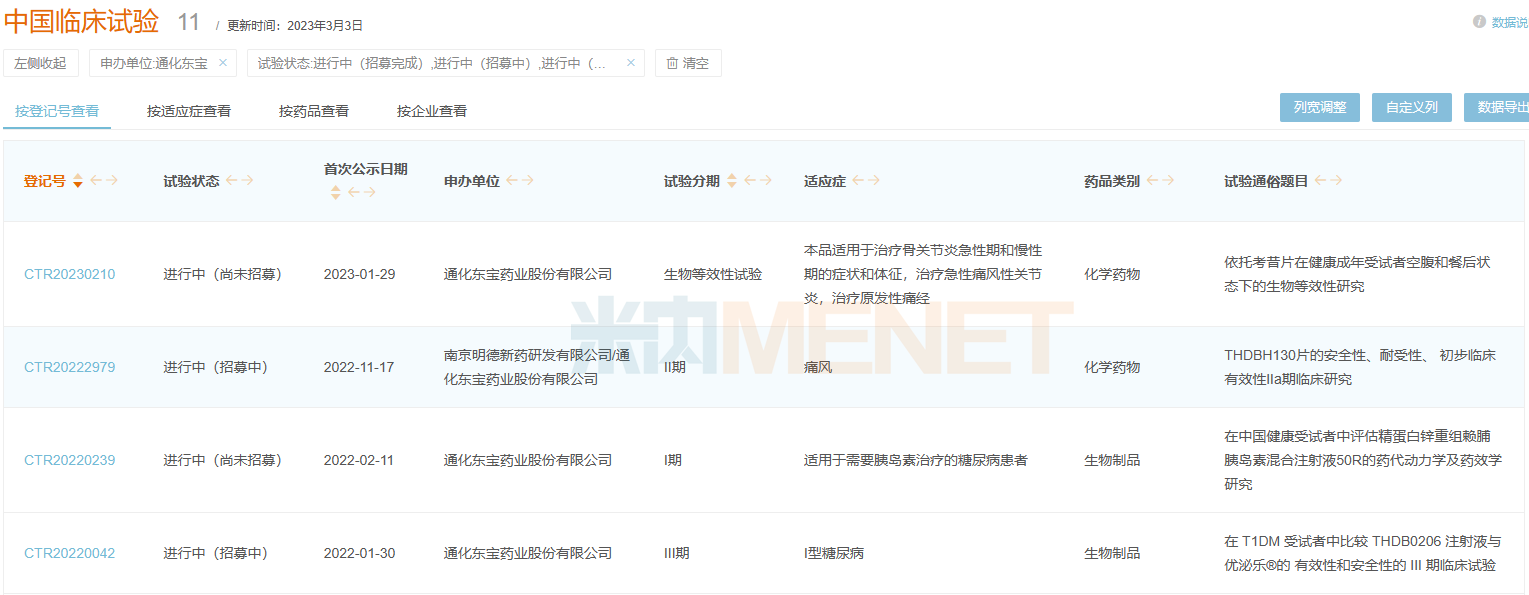

來源:米內(nèi)網(wǎng)新版數(shù)據(jù)庫
通化東寶深耕糖尿病治療領(lǐng)域,在不斷鞏固國產(chǎn)胰島素龍頭地位的同時,優(yōu)化在研產(chǎn)品結(jié)構(gòu),實現(xiàn)對胰島素類似物注射液、GLP-1受體激動劑、高臨床價值口服降糖藥品研發(fā)的全覆蓋。公司2022年前三季度研發(fā)費用1.12億元,占營收比例超過5%,研發(fā)費用已超過2020年全年。
通化東寶聚焦創(chuàng)新研發(fā),布局前沿靶點及療法,擴大產(chǎn)品適應(yīng)癥、拓展治療領(lǐng)域,在研項目中有3款糖尿病治療領(lǐng)域1類新藥、2款痛風(fēng)/高尿酸血癥治療領(lǐng)域1類新藥以及痛風(fēng)治療領(lǐng)域化學(xué)口服藥物。在研產(chǎn)品中的THDBH120/121、THDBH110/111、索馬魯肽注射液等品種涵蓋降糖、減肥等多個適應(yīng)癥。
值得注意的是,通化東寶近年積極拓展布局痛風(fēng)/高尿酸血癥領(lǐng)域,將結(jié)合公司現(xiàn)有的糖尿病慢病管理平臺,未來將形成良好的協(xié)同效應(yīng)。去年9月,公司的化藥1類新藥THDBH151片獲批臨床,該產(chǎn)品是痛風(fēng)雙靶點抑制劑,此前國內(nèi)外均暫無同類產(chǎn)品上市。
3大重磅新品沖擊超600億市場,20億大品種搶國產(chǎn)首家
2022年通化東寶獲批產(chǎn)品情況
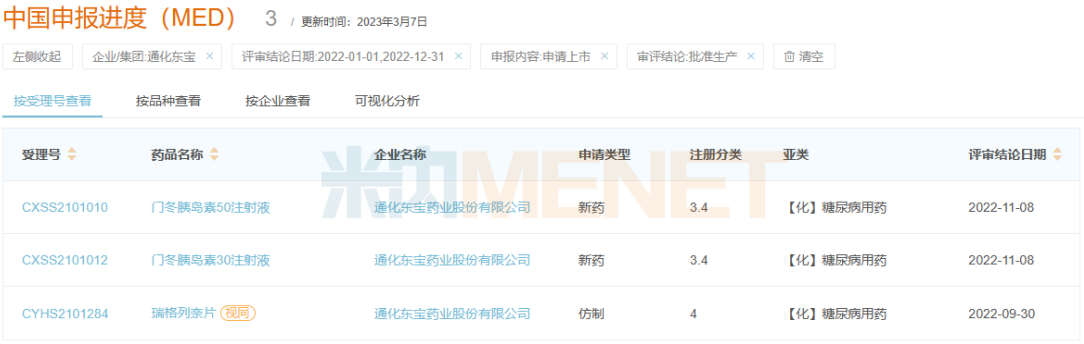
來源:米內(nèi)網(wǎng)新版數(shù)據(jù)庫
2022年,通化東寶有門冬胰島素50注射液、門冬胰島素30注射液、瑞格列奈片3款新品獲批,進一步豐富公司在糖尿病用藥領(lǐng)域的產(chǎn)品管線。米內(nèi)網(wǎng)數(shù)據(jù)顯示,2021年三大終端6大市場糖尿病用藥市場規(guī)模超過600億元。
瑞格列奈片是通化東寶第3款獲批的口服降糖藥,在此之前,公司已拿下磷酸西格列汀片和西格列汀二甲雙胍片(Ⅱ),均在2021年獲批。門冬胰島素50注射液和門冬胰島素30注射液獲批則實現(xiàn)公司在門冬胰島素系列產(chǎn)品的布局,其中,門冬胰島素50注射液是國產(chǎn)首家,2021年三大終端6大市場門冬胰島素合計銷售規(guī)模超過90億元。
通化東寶產(chǎn)品報產(chǎn)在審情況
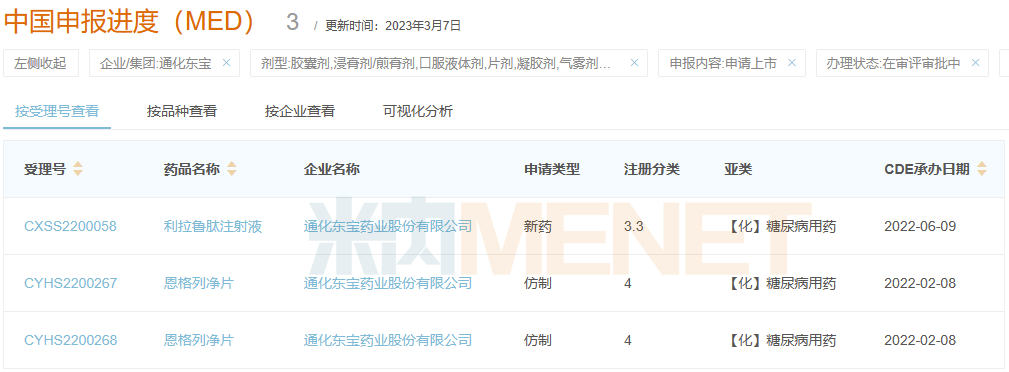
來源:米內(nèi)網(wǎng)新版數(shù)據(jù)庫
目前,通化東寶的有2款報產(chǎn)在審。2021年三大終端6大市場利拉魯肽注射液銷售規(guī)模近20億元;恩格列凈片則潛力驚人,2020年-2021年銷售額分別同比增長324.45%、179.51%。
近年三大終端6大市場利拉魯肽注射液銷售情況(單位:萬元)
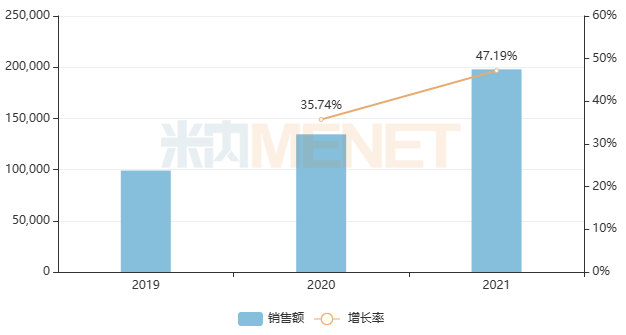
來源:米內(nèi)網(wǎng)格局數(shù)據(jù)庫
利拉魯肽是一種人胰高血糖素樣肽-1(GLP-1)類似物,可激活人GLP-1受體,促進胰腺分泌胰島素。該品種由諾和諾德研發(fā),2011年進入中國市場。2021年三大終端6大市場銷售額近20億元,同比增長超過40%。目前,國內(nèi)僅有諾和諾德?lián)碛猩a(chǎn)批文,通化東寶、杭州中美華東制藥、江蘇正大天晴藥業(yè)等6家報產(chǎn)在審。
資料顯示,2018年9月,通化東寶獲得國家藥監(jiān)局核準簽發(fā)的利拉魯肽原料藥審批意見通知件、利拉魯肽注射液藥物臨床試驗批件;2020年7月,獲得Ⅰ期臨床試驗總結(jié)報告;2021年10月,獲得Ⅲ期臨床試驗總結(jié)報告;2022年6月,利拉魯肽注射液報產(chǎn)獲受理,公司在該項目已投入研發(fā)費用超過2億元。
2022年12月,通化東寶與科興制藥簽署《利拉魯肽海外市場獨家許可合作協(xié)議》,科興制藥獲得利拉魯肽在新興市場共17個國家的獨家商業(yè)化許可權(quán)益。日前,科興制藥接受機構(gòu)調(diào)研時表示,該產(chǎn)品預(yù)期在2023年Q4在國內(nèi)獲批,公司正在推進利拉魯肽在海外市場的客戶篩選工作,產(chǎn)品獲批上市后將迅速啟動海外注冊。
多渠道布局,國產(chǎn)胰島素揚帆出海

今年以來,通化東寶捷報頻傳,多渠道布局,國產(chǎn)胰島素揚帆出海。GLP-1/GIP雙受體激動劑(注射用THDBH121)申報臨床、人胰島素注射液在歐盟申報上市均獲受理。
1月,化藥1類新藥GLP-1/GIP雙受體激動劑(注射用THDBH121)申報臨床獲受理,該產(chǎn)品是胰高血糖素樣肽-1(GLP-1)受體和葡萄糖促胰島素分泌多肽(GIP)受體雙靶點激動劑,其將GLP-1和GIP這兩種促胰島素的作用整合至一個多肽單分子中,且通過分子設(shè)計進一步提高代謝穩(wěn)定性,發(fā)揮協(xié)同促進的血糖控制、體重減輕以及調(diào)節(jié)脂質(zhì)代謝等功能,滿足單一分子靶點或復(fù)方制劑治療效果不佳的糖尿病患者的臨床需求,有望成為更長效的治療糖尿病和肥胖的重磅藥物。
2月,人胰島素注射液在歐盟申報上市獲受理,通化東寶負責(zé)提供胰島素原料藥,瑞康公司使用通化東寶提供的胰島素原料藥生產(chǎn)人胰島素注射液。通化東寶表示,公司近年穩(wěn)步推進人胰島素及胰島素類似物的海外注冊工作,該產(chǎn)品如順利獲批,將成為公司胰島素產(chǎn)品積極開拓發(fā)達國家市場的里程碑事件,同時加速公司人胰島素產(chǎn)品在海外多個國家的注冊進程,促進公司人胰島素產(chǎn)品的海外銷售,進一步開拓國際市場空間。
資料來源:公司公告、米內(nèi)網(wǎng)數(shù)據(jù)庫
注:米內(nèi)網(wǎng)《中國三大終端6大市場藥品競爭格局》,統(tǒng)計范圍是:城市公立醫(yī)院和縣級公立醫(yī)院、城市社區(qū)中心和鄉(xiāng)鎮(zhèn)衛(wèi)生院、城市實體藥店和網(wǎng)上藥店,不含民營醫(yī)院、私人診所、村衛(wèi)生室,不含縣鄉(xiāng)村藥店;上述銷售額以產(chǎn)品在終端的平均零售價計算。如有疏漏,歡迎指正!

