9月16日訊 9月10日,麗珠集團(tuán)公告稱,公司歷經(jīng)5年研發(fā)的注射用醋酸奧曲肽微球獲批臨床,該產(chǎn)品為長效緩釋制劑,目前國內(nèi)僅有進(jìn)口批文,公司累計投入研發(fā)費(fèi)用約2696萬元。2020上半年,麗珠集團(tuán)的獨(dú)家產(chǎn)品注射用醋酸亮丙瑞林微球?qū)崿F(xiàn)收入5.36億元,逆勢增長17.26%,目前公司的微球平臺在研新品注射用醋酸曲普瑞林微球、注射用阿立哌唑微球有望于2022年后陸續(xù)上市,成為拉升業(yè)績的新助力。今年上半年,疫情影響了全球經(jīng)濟(jì),麗珠集團(tuán)卻交出了營業(yè)收入、凈利潤雙漲的成績單,哪些爆款逆勢上漲,下半年又將有哪些重磅推出?
半年凈利潤首破10億,獨(dú)家注射劑暴漲4倍
數(shù)據(jù)顯示,2020上半年A股市場醫(yī)藥制造258家上市公司中,凈利潤超過10億元的僅有14家,麗珠集團(tuán)成功擠進(jìn)了營業(yè)收入、凈利潤雙增長的8家藥企名單之中。公司上半年營業(yè)收入50.95億元,同比增長3.16%,凈利潤10.05億元,同比增長35.97%。
圖1:2020H1銷售過億的制劑產(chǎn)品情況(單位:億元)
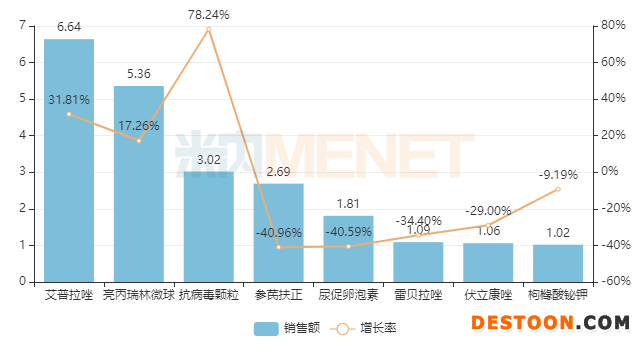
來源:公司公告
公司業(yè)績增長主要由獨(dú)家產(chǎn)品艾普拉唑貢獻(xiàn),其中腸溶片劑收入4.09億元,同比下滑10.45%,但注射用艾普拉唑鈉通過去年下半年的醫(yī)保談判進(jìn)入國家醫(yī)保目錄后,開始實(shí)現(xiàn)快速增量,收入達(dá)到2.55億元,同比增長437.85%;注射用醋酸亮丙瑞林微球收入5.36億元,逆勢實(shí)現(xiàn)17.26%的增長;抗病毒顆粒受新冠疫情治療需求提升的影響,實(shí)現(xiàn)收入3.02億元,同比增長78.24%;2019版國家目錄新增品種哌羅匹隆是麗珠集團(tuán)的獨(dú)家產(chǎn)品,上半年實(shí)現(xiàn)收入4546萬元,同比增長83.36%。
中藥注射劑大品種參芪扶正注射液是麗珠集團(tuán)的獨(dú)家產(chǎn)品,曾經(jīng)也是公司的風(fēng)云產(chǎn)品,受到政策影響,近幾年銷售下滑明顯,2018年全年銷售額在10億元左右,2019下滑至8億元,2020上半年僅為2.69億元。
疫情帶動試劑大漲,子公司欲獨(dú)立上市
麗珠集團(tuán)能在2020上半年獲得營收、凈利潤雙豐收的成績,除了拳頭產(chǎn)品銷售快速增長外,診斷試劑及設(shè)備板塊的成績也是十分耀眼。
2020年3月中旬,子公司麗珠試劑的新型冠狀病毒(2019-nCoV)IgM/IgG抗體檢測試劑盒(膠體金法)于國內(nèi)獲批上市,隨后又取得歐盟CE認(rèn)證,具備歐盟市場準(zhǔn)入條件,并在多個國家申請進(jìn)口注冊。隨著海外疫情大面積爆發(fā),新冠檢測試劑產(chǎn)品出口市場需求大幅增加,為集團(tuán)整體業(yè)績增長提供了重要支持,上半年診斷試劑及設(shè)備板塊共計實(shí)現(xiàn)銷售收入8.89億元,同比增長143.35%,占集團(tuán)總營收的比例上漲至17.45%,而由于出口單價更高,毛利率整體提升至76.48%。
圖2:麗珠集團(tuán)診斷試劑及設(shè)備板塊營收情況(單位:億元)
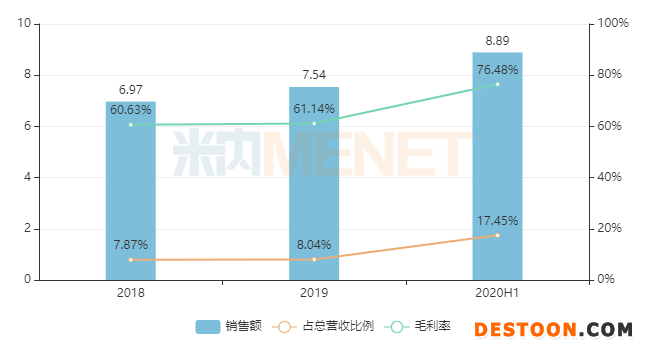
來源:公司年報
隨著新冠試劑產(chǎn)品順利出口帶來了紅利,子公司麗珠試劑也成立了海外銷售事業(yè)部,為未來其他試劑產(chǎn)品拓展海外市場奠定基礎(chǔ)。截至2020年6月30日,共有15個在產(chǎn)品種完成了歐盟CE的注冊工作。
在試劑研發(fā)上,2020上半年白介素IL-6測定試劑盒(化學(xué)發(fā)光法)、HBV核酸檢測試劑、HCV核酸檢測試劑、HBV核酸檢測試劑(一步法)、60速單人份化學(xué)發(fā)光分析儀、肌炎5項(xiàng)目自身抗體檢測試劑盒(磁條碼免疫熒光法)、血管炎3項(xiàng)自身抗體檢測試劑盒(磁條碼免疫熒光法)、抗核抗體檢測試劑盒(磁條碼免疫熒光法)(ANA-17)均已獲注冊證。
2020年8月10日,麗珠集團(tuán)公布了擬分拆麗珠試劑于A股上市的預(yù)案,分拆完成后公司股權(quán)結(jié)構(gòu)不會發(fā)生變化,麗珠集團(tuán)仍然持有麗珠試劑39.43%的股份,將維持對麗珠試劑的控制權(quán)。本次分拆上市有利于麗珠試劑拓寬融資渠道,進(jìn)一步建立在IVD(體外診斷)領(lǐng)域的品牌影響力,提升運(yùn)營效率與盈利能力;同時也有助于集團(tuán)進(jìn)一步聚焦主營,積極進(jìn)行創(chuàng)新藥和高壁壘仿制藥研發(fā)。
近幾年,隨著醫(yī)療保障的投入、消費(fèi)水平的提高,我國體外診斷試劑行業(yè)已經(jīng)進(jìn)入成長期,有數(shù)據(jù)顯示,2018年我國體外診斷試劑市場規(guī)模達(dá)到了604億元,2020年在新冠疫情帶動下,相關(guān)上市藥企的業(yè)績均得到“補(bǔ)位”,全年市場規(guī)模有望再創(chuàng)新高。麗珠試劑分拆上市后,最終能成就多高市值,我們拭目以待。
生物藥進(jìn)入收獲期:2個1類新藥獲批臨床,1個“國內(nèi)首家”即將上市
麗珠集團(tuán)上半年研發(fā)支出總額約3.50億元,同比增加1.63%,占總收入比例6.87%,保持著較為穩(wěn)定的研發(fā)投入強(qiáng)度。上半年,混合糖電解質(zhì)注射液獲批上市,米內(nèi)網(wǎng)數(shù)據(jù)顯示,該產(chǎn)品2019年在中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機(jī)構(gòu))終端總市場規(guī)模超過6億;公司重點(diǎn)產(chǎn)品維三聯(lián)(枸櫞酸鉍鉀片/替硝唑片/克拉霉素片)的重要組成部分之一替硝唑片通過一致性評價;兩個微球產(chǎn)品獲批臨床,均為國內(nèi)首家申報,其中注射用阿立哌唑微球處于I期臨床研究階段;兩個治療用生物制品1類新藥獲批臨床,同屬抗腫瘤和免疫調(diào)節(jié)劑,正在準(zhǔn)備啟動I期臨床。
表1:2020年至今麗珠獲批的重磅產(chǎn)品情況

來源:米內(nèi)網(wǎng)MED2.0中國藥品審評數(shù)據(jù)庫
近年來,麗珠集團(tuán)在重點(diǎn)布局微球平臺,2020年8月26日公司公告稱,擬以自有資金向麗珠微球公司增資2.09億元,麗珠制藥廠以其擁有的微球制劑相關(guān)生產(chǎn)性資產(chǎn)向麗珠微球增資1.39億元,欲將麗珠微球作為公司旗下微球相關(guān)產(chǎn)品的主要研發(fā)和生產(chǎn)平臺。
表2:2019年至今麗珠在審的上市申請及一致性評價補(bǔ)充申請情況
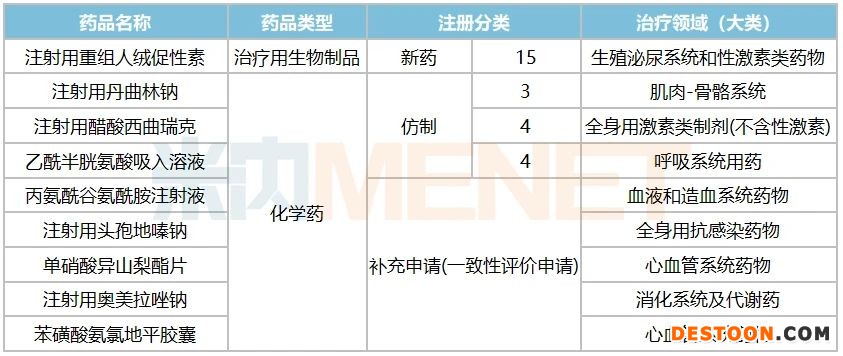
來源:米內(nèi)網(wǎng)MED2.0中國藥品審評數(shù)據(jù)庫
目前國內(nèi)市場上僅有默克雪蘭諾的重組人絨促性素注射液獲批進(jìn)口,國內(nèi)藥企中,麗珠集團(tuán)為首家申報注射用重組人絨促性素上市,并在審評審批中。原研產(chǎn)品適用于接受輔助生殖技術(shù)如體外授精(IVF)之前進(jìn)行超排卵的婦女,注射該產(chǎn)品可在刺激卵泡生長后觸發(fā)最終的卵泡成熟和黃體化;無排卵或少排卵婦女注射該產(chǎn)品可在剌激卵泡生長后觸發(fā)排卵及黃體化。麗珠集團(tuán)在半年報中提到,注射用重組人絨促性素于2020年6月初通過了藥品注冊生產(chǎn)現(xiàn)場核查,注冊檢驗(yàn)進(jìn)行中;此外,該產(chǎn)品的海外銷售準(zhǔn)備工作已開啟,在開展注冊準(zhǔn)備工作的同時,也在韓國、俄羅斯、埃及、南非、美國等地區(qū)開展初步商業(yè)洽談。
仿制藥方面,2019年至今在審的三個產(chǎn)品注射用丹曲林鈉、注射用醋酸西曲瑞克、乙酰半胱氨酸吸入溶液有望迎來新突破。注射用丹曲林鈉為罕見病用藥,用于治療惡性高熱,麗珠集團(tuán)于2015年按(原)化學(xué)藥品第3.3類申報臨床并于2017年獲批,2019年2月申報3類仿制上市,同年4月成功被納入優(yōu)先審評程序,目前國內(nèi)僅有麗珠集團(tuán)申報上市,拿下首仿是大概率事件。
注射用醋酸西曲瑞克原研企業(yè)為默沙東,目前國內(nèi)已有深圳翰宇藥業(yè)獲批,但暫無企業(yè)過評,目前按新分類申報上市的僅有麗珠集團(tuán),若順利獲批則成為首家過評企業(yè)。2019年注射用醋酸西曲瑞克在中國公立醫(yī)療機(jī)構(gòu)終端銷售額接近2.5億元。
乙酰半胱氨酸吸入劑暫無企業(yè)過評,目前按新分類申報上市并在審的企業(yè)除了麗珠集團(tuán)還有康緣藥業(yè)、吳中醫(yī)藥集團(tuán)等5家,首家過評最終花落誰家?2019年乙酰半胱氨酸吸入劑在中國公立醫(yī)療機(jī)構(gòu)終端銷售額超過8億元。
結(jié)語
2020下半年,麗珠集團(tuán)將針對二級以上醫(yī)院,推進(jìn)艾普拉唑組合在醫(yī)療機(jī)構(gòu)的開發(fā),繼續(xù)擴(kuò)大艾普拉唑的銷售規(guī)模;全力確保注射用重組人絨促性素的順利獲批上市,以及全面策劃該產(chǎn)品上市后的市場布局;診斷試劑及設(shè)備方面,爭取按計劃完成血液輻照儀、自免多重儀器、60速發(fā)光儀器、核酸設(shè)備及配套試劑的市場布局,為2021年的銷售增長奠定基礎(chǔ)。
來源:公司年報、米內(nèi)網(wǎng)數(shù)據(jù)庫
審評數(shù)據(jù)統(tǒng)計截至2020年9月15日,如有錯漏,敬請指正。



 110102000668(1)號
110102000668(1)號