8月24日訊 8月21日,CDE官網(wǎng)數(shù)據(jù)顯示,石家莊格瑞藥業(yè)的鹽酸阿羅洛爾片4類仿制上市申請獲得承辦。鹽酸阿羅洛爾片原研企業(yè)為日本住友,目前國內(nèi)市場僅有進(jìn)口批文。
圖1:石家莊格瑞藥業(yè)的鹽酸阿羅洛爾片的注冊情況
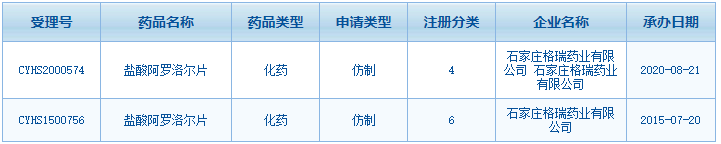
來源:CDE官網(wǎng)
圖2:鹽酸阿羅洛爾片的銷售情況
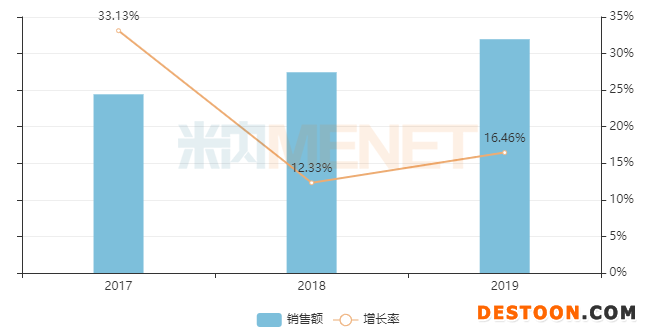
來源:米內(nèi)網(wǎng)中國公立醫(yī)療機(jī)構(gòu)終端競爭格局
鹽酸阿羅洛爾片為第3代β受體阻滯劑,用于治療原發(fā)性高血壓(輕-中度),心絞痛,心動過速性心律失常,原發(fā)性震顫。資料顯示,該產(chǎn)品于1985年在日本上市,1995年登陸中國市場,目前是國家醫(yī)保目錄乙類品種,2019年在中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機(jī)構(gòu))終端銷售額接近2億元。
圖3:鹽酸阿羅洛爾片臨床情況

來源:米內(nèi)網(wǎng)中國藥品臨床試驗公示庫
原研在中國上市超過20年,國產(chǎn)仿制藥竟然是一片空白?米內(nèi)網(wǎng)數(shù)據(jù)顯示,石家莊格瑞藥業(yè)在2015年7申報6類仿制上市,于2016年10月獲批臨床,2019年7月完成了BE,近期申報4類仿制上市獲得受理。目前僅有1家企業(yè)申報上市,“獨市之爭”能否堅持到首仿獲批?我們拭目以待。
來源:CDE官網(wǎng)、米內(nèi)網(wǎng)數(shù)據(jù)庫
審評數(shù)據(jù)統(tǒng)計截至2020年8月21日,如有錯漏,敬請指正。



 110102000668(1)號
110102000668(1)號