8月21日訊 8月18日,華東醫(yī)藥發(fā)布公告稱,公司全資子公司中美華東將對(duì)荃信生物進(jìn)行3.7億元的股權(quán)投資,獲得后者20.56%的股權(quán),同時(shí)與該公司簽訂QX001S在中國(guó)大陸的合作開發(fā)和商業(yè)化協(xié)議。華東醫(yī)藥目前處于轉(zhuǎn)型升級(jí)階段,4個(gè)1類新藥在研,最快已開展至III期臨床。
QX001S是根據(jù)NMPA、FDA、EMA生物類似藥相關(guān)指導(dǎo)原則開發(fā)的全球首個(gè)烏司奴單抗生物類似藥。烏司奴單抗是由強(qiáng)生研制的全球首個(gè)全人源“雙靶向”IL-12和IL-23的重組全人源化單克隆抗體注射液,目前獲批的適應(yīng)癥包括中重度斑塊型銀屑病、中重度克羅恩?。–D)、活動(dòng)性銀屑病關(guān)節(jié)炎、中重度活動(dòng)性潰瘍性結(jié)腸炎(UC)等。
圖1:強(qiáng)生的烏司奴單抗注射液全球銷售情況(單位:百萬美元)
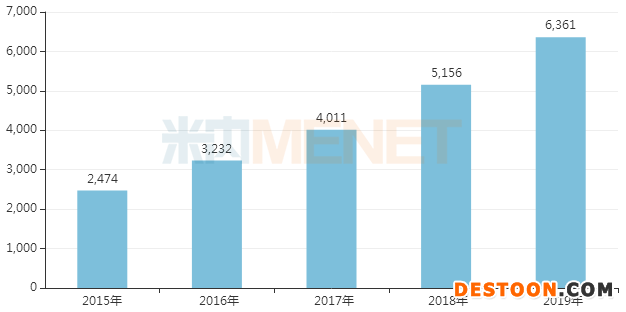
來源:米內(nèi)網(wǎng)跨國(guó)上市公司銷售數(shù)據(jù)庫(kù)
烏司奴單抗注射液為強(qiáng)生的當(dāng)家產(chǎn)品,近幾年來在全球的銷售額保持快速增長(zhǎng)的態(tài)勢(shì),2019年實(shí)現(xiàn)銷售收入63.61億美元,2020上半年在疫情影響之下仍逆勢(shì)增長(zhǎng)18.7%,銷售收入達(dá)到35.16億美元。
目前全球范圍內(nèi)尚無烏司奴單抗生物類似藥獲批,國(guó)內(nèi)也僅有荃信生物(QX001S注射液)、百奧泰(BAT2206注射液)兩家公司的產(chǎn)品先后獲批臨床。
圖2:QX001S注射液國(guó)內(nèi)臨床試驗(yàn)登記情況
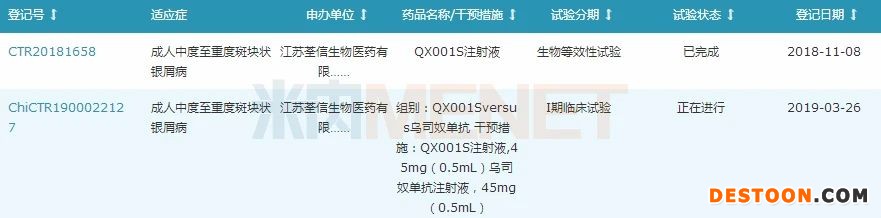
來源:米內(nèi)網(wǎng)中國(guó)藥品臨床試驗(yàn)公示庫(kù)
QX001S注射液于2018年獲得臨床批件并完成I期臨床首例受試者給藥,研發(fā)進(jìn)度在全球范圍內(nèi)處于領(lǐng)先地位,荃信生物計(jì)劃于2021年初啟動(dòng)QX001S治療成人中重度斑塊狀銀屑病的III期研究,華東醫(yī)藥未來有望收獲一個(gè)重磅單抗生物類似藥。
隨著國(guó)內(nèi)醫(yī)藥市場(chǎng)環(huán)境發(fā)生深刻變革,華東醫(yī)藥在“轉(zhuǎn)型創(chuàng)新”戰(zhàn)略之下將“內(nèi)分泌、自身免疫疾病、腫瘤”三大疾病領(lǐng)域確定為創(chuàng)新產(chǎn)品布局的核心方向,力爭(zhēng)2022年開始,保持每年有創(chuàng)新產(chǎn)品上市的良性發(fā)展節(jié)奏,實(shí)現(xiàn)2025年創(chuàng)新業(yè)務(wù)板塊占整體工業(yè)營(yíng)收30%的階段性目標(biāo)。
表:華東醫(yī)藥在研的1類新藥
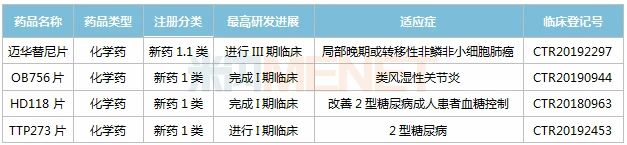
來源:米內(nèi)網(wǎng)中國(guó)藥品臨床試驗(yàn)公示庫(kù)
米內(nèi)網(wǎng)數(shù)據(jù)顯示,目前華東醫(yī)藥有4個(gè)1類新藥在研,均屬于化學(xué)藥,其中邁華替尼片進(jìn)展最快,治療局部晚期或轉(zhuǎn)移性非鱗非小細(xì)胞肺癌的III期臨床試驗(yàn)已啟動(dòng),該產(chǎn)品屬于第二代EGFR-TKI靶向藥,公司爭(zhēng)取以邁華替尼用于一/二線罕見基因突變的II期單臂臨床試驗(yàn)結(jié)果直接申報(bào)上市。
TTP273片為華東醫(yī)藥引進(jìn)的口服GLP-1創(chuàng)新藥,2型糖尿病適應(yīng)癥已開展I期臨床;HD118片為公司技術(shù)轉(zhuǎn)讓來的DPP-4抑制劑,改善2型糖尿病成人患者血糖控制適應(yīng)癥已完成I期臨床;OB756片類風(fēng)濕性關(guān)節(jié)炎適應(yīng)癥已完成I期臨床,骨髓增殖性疾病適應(yīng)癥已獲批臨床。
來源:米內(nèi)網(wǎng)數(shù)據(jù)庫(kù)、上市公司公告
注:數(shù)據(jù)統(tǒng)計(jì)截至8月19日,如有疏漏,歡迎指正!



 110102000668(1)號(hào)
110102000668(1)號(hào)