日前,杭州朱養(yǎng)心藥業(yè)提交的痛風(fēng)藥非布司他片一致性評價獲得批準(zhǔn)。近幾年來隨著人們生活水平提升,飲食結(jié)構(gòu)變化,痛風(fēng)發(fā)病率逐年上升。米內(nèi)網(wǎng)數(shù)據(jù)顯示,2019年中國公立醫(yī)療機(jī)構(gòu)終端痛風(fēng)藥市場首次突破20億元,2015-2019年5年復(fù)合增速達(dá)49.8%;3個痛風(fēng)藥有企業(yè)布局一致性評價,其中別嘌醇片還未有企業(yè)過評;據(jù)不完全統(tǒng)計,目前國內(nèi)有14個國產(chǎn)痛風(fēng)1類新藥在研,其中恒瑞醫(yī)藥進(jìn)展最快;托匹司他片進(jìn)口臨床申請已獲批,成都倍特、人福等15家企業(yè)的仿制藥也獲批臨床。
5年復(fù)合增長近50%,4大痛風(fēng)藥壟斷市場
近幾年來,隨著人們生活水平提升,飲食結(jié)構(gòu)改變,痛風(fēng)的發(fā)病率逐年上升且呈年輕化趨勢,成為繼高血壓、高血糖、高血脂后的第四類慢性病。米內(nèi)網(wǎng)數(shù)據(jù)顯示,2019年中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機(jī)構(gòu))終端抗痛風(fēng)制劑市場首次突破20億元,2015-2019年5年復(fù)合增速達(dá)49.8%。
圖:中國公立醫(yī)療機(jī)構(gòu)終端抗痛風(fēng)制劑TOP4通用名藥品
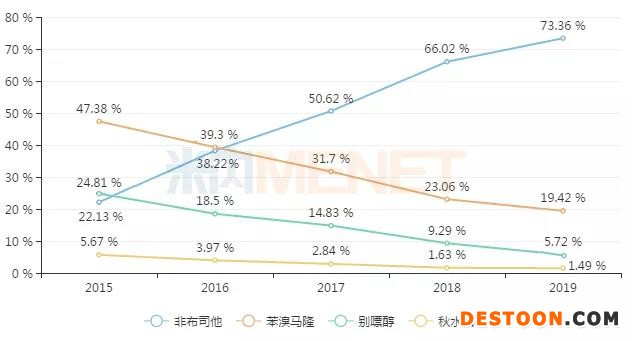
目前國內(nèi)市場常用的痛風(fēng)藥有非布司他、苯溴馬隆、別嘌醇、秋水仙堿及丙磺舒,其中前4個品種在2019年中國公立醫(yī)療機(jī)構(gòu)終端合計市場份額為99.99%,非布司他以73.36%的市場份額遙遙領(lǐng)先。
非布司他是一種選擇性黃嘌呤氧化酶/黃嘌呤脫氫酶抑制劑,依靠其降尿酸作用強、過敏反應(yīng)少、不額外加重腎臟負(fù)擔(dān)等特點成為目前臨床首選的降尿酸藥。米內(nèi)網(wǎng)數(shù)據(jù)顯示,近幾年來非布司他在中國公立醫(yī)療機(jī)構(gòu)終端的銷售逐年上漲,近5年復(fù)合增長率達(dá)102.14%,在抗痛風(fēng)制劑整體市場所占比重逐年遞增。除原研廠家日本帝人外,還有江蘇萬邦生化、恒瑞醫(yī)藥、杭州朱養(yǎng)心藥業(yè)3家企業(yè)的仿制藥獲批上市。
苯溴馬隆屬于促進(jìn)尿酸排泄藥,價格相對便宜,曾經(jīng)也在抗痛風(fēng)制劑市場獨領(lǐng)風(fēng)騷,但由于其對腎臟負(fù)擔(dān)大、肝損害問題比較突出,市場逐漸被非布司他擠占。近幾年來苯溴馬隆在中國公立醫(yī)療機(jī)構(gòu)終端銷售額雖保持增長,但在抗痛風(fēng)制劑整體市場所占比重逐年下降。國內(nèi)上市銷售的苯溴馬隆劑型有片劑及膠囊劑,其中片劑占90%以上的市場份額。
別嘌醇可以直接抑制人體體內(nèi)尿酸生成,降低血及尿中的尿酸水平,不會額外增加腎臟負(fù)擔(dān),但過敏發(fā)生率較高,近年來在臨床上的應(yīng)用逐漸受到限制,2019年在中國公立醫(yī)療機(jī)構(gòu)終端銷售額超過1億元,同比下滑22.95%。
秋水仙堿是預(yù)防復(fù)發(fā)性痛風(fēng)性關(guān)節(jié)炎急性發(fā)作的藥物,雖然相對于非布司他、苯溴馬隆,擁有秋水仙堿制劑生產(chǎn)批文的企業(yè)數(shù)較多,但其銷售市場一直處于不溫不火的狀態(tài),隨著其他痛風(fēng)藥的崛起,秋水仙堿在抗痛風(fēng)制劑整體市場所占比重逐年下降。
在研痛風(fēng)新藥備受矚目,恒瑞沖刺首個國產(chǎn)1類新藥
目前國內(nèi)痛風(fēng)治療藥物的研究通?;谀I小管對尿酸重吸收的代謝步驟,從促進(jìn)尿酸排出和抑制尿酸生成兩方面入手,其中通過抑制尿酸鹽重吸收轉(zhuǎn)運子1(URAT1)促進(jìn)尿酸的排泄是目前的熱點研究靶點。
表1:痛風(fēng)新藥國內(nèi)在研情況
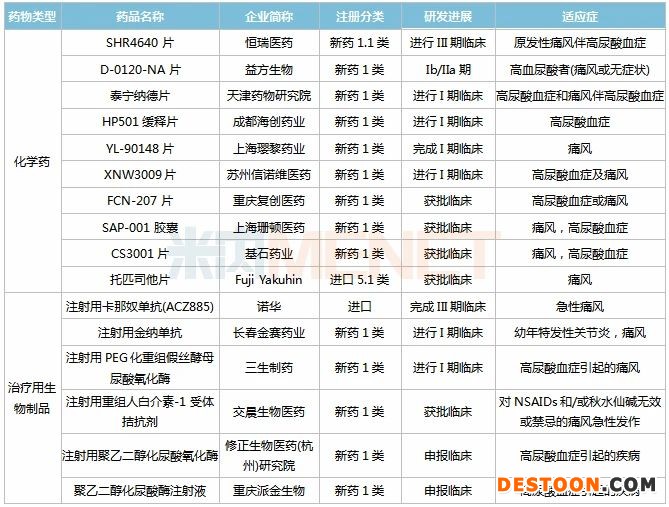
米內(nèi)網(wǎng)數(shù)據(jù)顯示,目前國內(nèi)在研的1類痛風(fēng)新藥中,恒瑞醫(yī)藥的SHR4640片進(jìn)展最快,該產(chǎn)品屬于新一代URAT1選擇性抑制劑,原發(fā)性痛風(fēng)伴高尿酸血癥適應(yīng)癥已在國內(nèi)開展III期臨床,有望成為國內(nèi)抗痛風(fēng)領(lǐng)域首個獲批的國產(chǎn)1類新藥。
阿斯利康的雷西納德(Lesinurad)是全球首個上市的URAT1抑制劑,由于其使用劑量高、腎臟毒性問題明顯,患者無法長期使用,目前僅獲批于聯(lián)合使用。SHR4640片有成為“Best in class”的潛力,基于URAT1抑制活性數(shù)據(jù),理論上達(dá)到相同抑制作用時,SHR4640片的用量僅約為雷西納德的1/215,這為SHR4640片低劑量治療、降低不良反應(yīng)提供了可能。
與SHR4640片同靶點的在研新藥還有益方生物的D-0120-NA片、上海瓔黎藥業(yè)的YL-90148片、成都海創(chuàng)藥業(yè)的HP501緩釋片、天津藥物研究院的泰寧納德片等,其中D-0120-NA片高血尿酸者(痛風(fēng)或無癥狀)適應(yīng)癥已開展Ib/IIa期臨床,進(jìn)度僅次于SHR4640片。
日本富士藥品的托匹司他是一種新型的高選擇性、可逆性黃嘌呤氧化酶抑制劑,通過競爭性的抑制黃嘌呤氧化酶,從而抑制尿酸的生成。該產(chǎn)品于2013年6月在日本獲批上市,2019年8月在國內(nèi)獲批臨床,用于治療痛風(fēng)。雖然原研還未獲批進(jìn)口,但已有不少國內(nèi)藥企布局仿制藥,以新藥3.1類提交托匹司他片臨床申請,其中人福、成都倍特、辰欣藥業(yè)等15家藥企的產(chǎn)品已獲批臨床。
諾華的注射用卡那奴單抗(ACZ885)是用于中和白介素-1β(IL-1β)的完全人源化單克隆抗體,IL-1β生成過多被認(rèn)為在許多炎癥性疾病中起重要作用,包括痛風(fēng)性關(guān)節(jié)炎。其急性痛風(fēng)的適應(yīng)癥在國內(nèi)已完成III期臨床,如若順利獲批,將成為國內(nèi)治療痛風(fēng)性關(guān)節(jié)炎疼痛和炎癥的新型療法。
15億大品種遭哄搶,華潤、上藥搶首家過評
表2:抗痛風(fēng)制劑一致性評價申報情況(含新分類報產(chǎn))
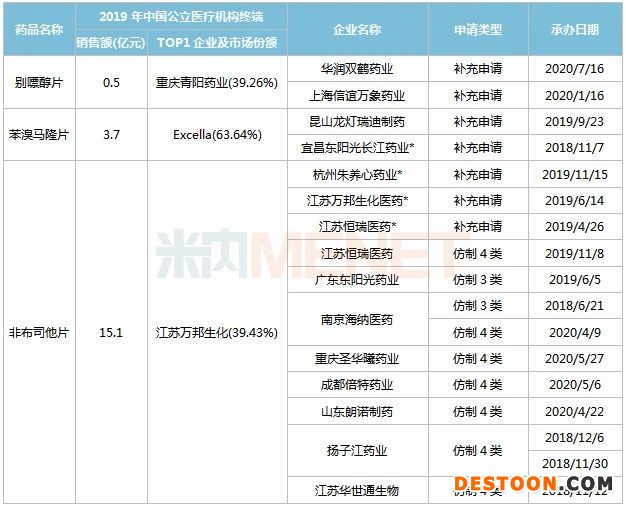
注:帶*為已過評
別嘌醇片、苯溴馬隆片、非布司他片3個痛風(fēng)藥已有企業(yè)提交一致性評價補充申請或以新分類報產(chǎn),其中苯溴馬隆片、非布司他片已有企業(yè)過評。
作為降尿酸治療的一線用藥,非布司他近年來市場增長強勁,國內(nèi)多家企業(yè)爭相仿制該產(chǎn)品。米內(nèi)網(wǎng)數(shù)據(jù)顯示,目前有10家企業(yè)提交非布司他片一致性評價補充申請或以新分類報產(chǎn),包括恒瑞、東陽光藥、揚子江等,其中恒瑞、江蘇萬邦生化醫(yī)藥、杭州朱養(yǎng)心藥業(yè)的產(chǎn)品已順利過評,恒瑞為國內(nèi)首家。
目前非布司他在國內(nèi)僅片劑上市銷售,但已有藥企布局其他劑型,杭州朱養(yǎng)心藥業(yè)、海正藥業(yè)等5家企業(yè)提交非布司他膠囊臨床申請,其中杭州朱養(yǎng)心藥業(yè)、山東百諾醫(yī)藥的產(chǎn)品已獲批臨床。
苯溴馬隆片有兩家藥企提交一致性評價補充申請,宜昌東陽光長江藥業(yè)的產(chǎn)品已順利獲批,為國內(nèi)首家;上海信誼萬象藥業(yè)、華潤雙鶴藥業(yè)提交別嘌醇片一致性評價補充申請,目前該產(chǎn)品還未有企業(yè)過評。
來源:米內(nèi)網(wǎng)數(shù)據(jù)庫
注:數(shù)據(jù)統(tǒng)計截至7月27日,如有疏漏,歡迎指正!



 110102000668(1)號
110102000668(1)號