
2020年07月18日訊 /生物谷BIOON/ --百濟神州(BeiGene)近日宣布,國家藥品監(jiān)督管理局(NMPA)藥品審評中心(CDE)已受理其在研PARP1和PARP2抑制劑pamiparib(帕米帕利)的新藥上市申請(NDA),該藥用于治療既往接受過至少兩線化療、攜有致病或疑似致病的胚系 BRCA 突變的晚期卵巢癌、輸卵管癌或原發(fā)性腹膜癌患者。
此次是百濟神州針對pamiparib遞交的首項新藥上市申請,同時也標志著該公司第三款自主研發(fā)產(chǎn)品進入藥政審批階段。今年6月初,百濟神州自主研發(fā)的新一代BTK抑制劑百悅澤(Brukinsa,通用名:zanubrutinib,澤布替尼)獲得國家藥監(jiān)局批準,成為國內(nèi)首個上市的國產(chǎn)BTK抑制劑,該藥之前于2019年11月獲得美國FDA批準,標志著中國原研抗癌新藥出海“零的突破”。
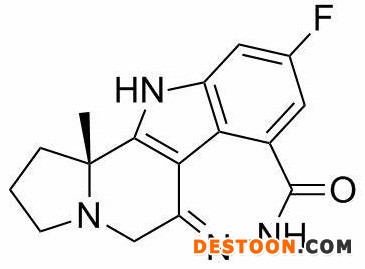
pamiparib化學(xué)結(jié)構(gòu)式(圖片來源:medchemexpress.com)
目前,百濟神州正在推進pamiparib的全球開發(fā)項目,評估其作為單藥或與包括抗PD-1抗體百澤安®(tislelizumab,替雷利珠單抗注射液)在內(nèi)的其他藥物聯(lián)合的潛能。pamiparib作為一款靶向治療藥物,將為中國的晚期卵巢癌患者帶來新的治療希望。該公司未來幾個月公布支持此次新藥上市申請的臨床數(shù)據(jù),以及包括3期數(shù)據(jù)在內(nèi)的其他臨床結(jié)果。
此次NDA,是基于一項pamiparib用于治療晚期卵巢癌、輸卵管癌、原發(fā)性腹膜癌或晚期三陰乳腺癌患者的1/2臨床試驗(NCT03333915)的結(jié)果。該試驗的關(guān)鍵性2期部分在中國入組了113例既往接受過至少兩項標準化療、攜有BRCA1/2突變的高級別上皮性卵巢癌(包括輸卵管癌或原發(fā)性腹膜癌)或高級別子宮內(nèi)膜上皮樣癌患者?;颊呓邮芰藀amiparib每日2次口服用藥、每次60mg的治療。該試驗的主要終點為基于實體腫瘤療效評估標準RECIST 1.1版的客觀緩解率(ORR)。試驗結(jié)果將在未來一場醫(yī)學(xué)會議上公布。
卵巢癌在中國女性常見癌癥排名中位列第十名。2018年,50000多名新增病例并有30000余名死亡病例。超過六成的卵巢癌患者在確診時已為晚期。卵巢癌的標準治療包括手術(shù)及術(shù)后鉑類藥物化療。在卵巢癌患者中,九成以上患有上皮性卵巢癌。其中,約有70%的上皮性卵巢癌患者在接受一線療法并獲得完全緩解后,仍將出現(xiàn)復(fù)發(fā)性疾病。
帕米帕利(pamiparib,BGB-290)是一款在研PARP1和PARP2抑制劑,臨床前模型顯示其具有穿透血腦屏障和PARP-DNA復(fù)合物捕捉等藥理學(xué)特性。由百濟神州的科學(xué)家在北京研發(fā)中心自主研發(fā),帕米帕利目前正作為單一療法或與其他藥物聯(lián)用治療多種惡性實體瘤進行全球臨床開發(fā)。迄今為止,已有1200多例患者入組帕米帕利臨床試驗。(生物谷Bioon.com)
原文出處:百濟神州



 110102000668(1)號
110102000668(1)號