10月9日訊 9月28日,華海藥業(yè)發(fā)布公告稱,下屬子公司華博生物的重組人血管內(nèi)皮生長因子受體-抗體融合蛋白眼用注射液(HB002.1M)項目3個新增適應(yīng)癥,獲國家藥監(jiān)局批準(zhǔn)臨床。截至目前,HB002.1M共有4個適應(yīng)癥(濕性年齡相關(guān)性黃斑變性、視網(wǎng)膜分支靜脈阻塞繼發(fā)黃斑水腫、視網(wǎng)膜中央靜脈阻塞繼發(fā)黃斑水腫和糖尿病黃斑水腫)獲批臨床。HB002.1M的首個適應(yīng)癥濕性年齡相關(guān)性黃斑變性試驗已進(jìn)展至II期臨床。
HB002.1M是一種以血管內(nèi)皮生長因子(VEGF)為靶點(diǎn)的重組融合蛋白,國內(nèi)外已上市同靶點(diǎn)、同治療領(lǐng)域藥物包括雷珠單抗、阿柏西普和康柏西普。米內(nèi)網(wǎng)數(shù)據(jù)顯示,2019年中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機(jī)構(gòu))終端眼科用藥銷售額超過110億元,同比增長16.62%。
中國公立醫(yī)療機(jī)構(gòu)終端眼科用藥銷售情況(單位:億元)
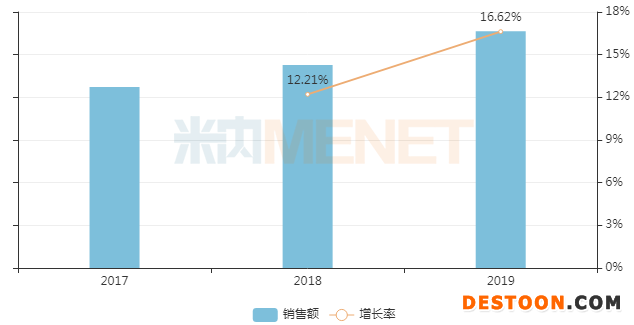
來源:米內(nèi)網(wǎng)中國公立醫(yī)療機(jī)構(gòu)終端競爭格局
今年以來,華海藥業(yè)已有3款1類新藥獲批臨床,分別為重組人血管內(nèi)皮生長因子受體-抗體融合蛋白眼用注射液、HOT-1030注射液、HB0017注射液。
2020年至今華海藥業(yè)子公司獲批臨床的1類新藥
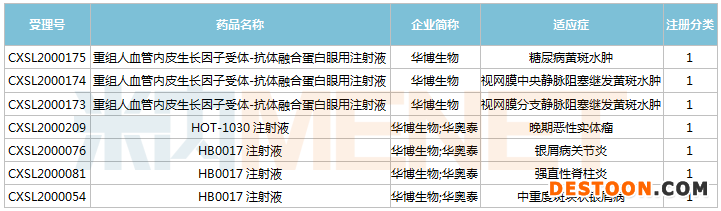
HOT-1030注射液是一種以CD137(4-1BB)為靶點(diǎn)的單克隆抗體,擬用于治療晚期惡性實(shí)體腫瘤。截至目前,以CD137(4-1BB)為靶點(diǎn)的藥物均尚未上市。
HB0017注射液是一種以白介素-17(IL-17)為靶點(diǎn)的單克隆抗體,擬用于治療銀屑病、銀屑病關(guān)節(jié)炎和強(qiáng)制性脊柱炎,IL-17是該類疾病的一個重要治療靶點(diǎn)。國內(nèi)外已上市同靶點(diǎn)(IL-17/IL-17 受體)藥物包括Cosentyx(司庫奇尤單抗)、Taltz(依奇珠單抗)。
9月29日,華海藥業(yè)發(fā)布前三季度業(yè)績預(yù)告,預(yù)計2020年1-9月實(shí)現(xiàn)凈利潤8.2億元-8.7億元,同比增長約60%-70%。業(yè)績預(yù)增的主要原因是國內(nèi)制劑及原料藥銷售大幅增加影響。
在國家開展的三批集采中,華海藥業(yè)累計有12個品種中選國家?guī)Я?strong>采購,集采中標(biāo)助力公司產(chǎn)品迅速打開市場,促進(jìn)國內(nèi)制劑銷售大幅增加。



 110102000668(1)號
110102000668(1)號